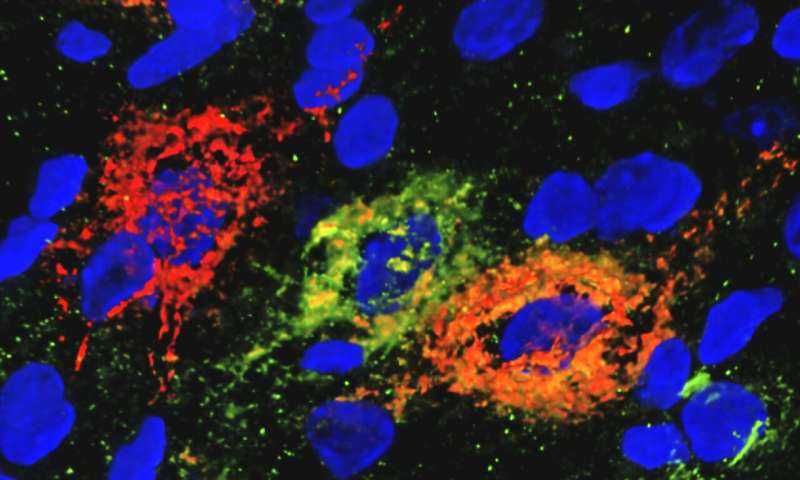
En roedores con diabetes tipo 2, una sola inyección quirúrgica de una proteína llamada factor de crecimiento de fibroblastos 1 puede restaurar los niveles de azúcar en sangre a la normalidad durante semanas o meses. Sin embargo, no se ha entendido bien cómo actúa este factor de crecimiento en el cerebro para generar este beneficio duradero.
por la Universidad de Washington
Aclarar cómo ocurre esto podría conducir a tratamientos para la diabetes más efectivos que aprovechen el potencial inherente del cerebro para mejorar la afección.
«Hasta hace poco, no se reconocía la capacidad del cerebro para normalizar los niveles elevados de azúcar en sangre en animales diabéticos», dijo el Dr. Michael Schwartz, profesor de medicina de la Facultad de Medicina de la Universidad de Washington y codirector del Instituto de Medicina de la Diabetes de la Universidad de Washington. «Al interrogar las respuestas celulares y moleculares inducidas en el hipotálamo por un péptido cerebral llamado factor de crecimiento de fibroblastos 1, los últimos hallazgos de nuestros equipos internacionales trazan un camino hacia una comprensión más completa de cómo se logra este efecto.
«Estos conocimientos», dijo, «algún día pueden informar las estrategias terapéuticas para inducir la remisión sostenida de la diabetes, en lugar de simplemente reducir los niveles de azúcar en la sangre todos los días como lo hacen los tratamientos actuales».
La diabetes tipo 2 afecta al 10% de la población de EE. UU. Está estrechamente relacionado con la obesidad y causa graves problemas de salud, como enfermedades cardíacas, pérdida de la visión, insuficiencia renal, demencia, infecciones difíciles de curar y daño a los nervios. También aumenta el riesgo de necesitar amputaciones. El control de los niveles de azúcar en sangre puede prevenir estos problemas, pero a menudo es difícil de lograr y se convierte en una lucha constante para muchos pacientes.
En dos artículos complementarios de las ediciones del 7 de septiembre de Nature Communications y Nature Metabolism , equipos internacionales de investigadores describen la intrincada biología de la respuesta del cerebro al factor de crecimiento de fibroblastos 1. El primer equipo describe respuestas celulares robustas que parecen salvaguardar las vías de señalización del cerebro. fundamental para mantener bajo control el azúcar en sangre.
Un segundo equipo, que incluía a algunos de los mismos investigadores, hizo descubrimientos sobre conjuntos de matrices extracelulares llamados » redes perineuronales » que enredan grupos de neuronas involucradas en el control del azúcar en sangre. Los investigadores descubrieron que el factor de crecimiento de fibroblastos 1 repara las mallas perineuronales que han sido dañadas por la diabetes. Esta respuesta es necesaria para que se mantenga la remisión de la diabetes.
El Dr. Tunes Pers, del Centro de Investigación Metabólica Básica de la Fundación Novo Nordisk, Universidad de Copenhague en Dinamarca, y el investigador de diabetes y obesidad Dr. Michael Schwartz de UW Medicine en Seattle fueron los autores principales del informe Nature Communications. Los autores principales de sus laboratorios fueron la Dra. Marie Bentsen y el Dr. Dylan Rausch.
El equipo internacional de científicos que reunieron comenzó detallando los cambios en la expresión génica inducidos por el tratamiento del factor de crecimiento de fibroblastos 1 en diversos tipos de células cerebrales ubicadas en el hipotálamo. Esta pequeña región del cerebro regula muchas funciones corporales, incluidos los niveles de azúcar en la sangre, el hambre, la ingesta de alimentos y el uso y almacenamiento de energía.
Los científicos descubrieron que las células gliales , que no solo brindan apoyo estructural sino que también ayudan a organizar y regular la actividad de los neurocircuitos, respondían con mayor intensidad que las neuronas, células cerebrales conocidas por la transmisión eléctrica de información.
Los investigadores también observaron interacciones mejoradas entre los astrocitos y un subconjunto de neuronas que producen proteínas relacionadas con agutí (llamadas neuronas Agrp). Los astrocitos son abundantes células gliales en forma de estrella que nutren a las neuronas y apoyan sus transmisiones eléctricas. Las neuronas Agrp son componentes esenciales del sistema de señalización de la melanocortina, un circuito cerebral crucial para controlar la alimentación, el peso corporal y el azúcar en sangre.
Se sabe que la activación excesiva de las neuronas Agrp amortigua la señalización de la melanocortina. Este efecto se ha relacionado con el desarrollo de diabetes en personas y roedores. Los investigadores observaron que prohibir la señalización de melancortina después de la inyección del factor de crecimiento de fibroblastos 1 en el cerebro previene la remisión sostenida de la diabetes.
Entre otros tipos de células que respondieron enérgicamente al factor de crecimiento de fibroblastos 1 se encuentran los tanicitos, células gliales alargadas sensibles a los nutrientes que se encuentran solo en el hipotálamo. Sus contribuciones a la normalización de los niveles de glucosa requieren un estudio adicional.
El artículo publicado en Nature Metabolism analizó las estructuras que los científicos llamaron «los participantes previamente no reconocidos» en el mecanismo detrás de la capacidad del factor de crecimiento de fibroblastos 1 para inducir la remisión de la diabetes.
Estas son las redes perineuronales que enredan las neuronas reguladoras del azúcar en sangre en el hipotálamo, incluidas las neuronas Agrp. El autor principal de este artículo es Kim Alonge, instructora interina de medicina en la Facultad de Medicina de la Universidad de Washington. El autor principal es Michael Schwartz.
Las redes perineuronales promueven la estabilidad de los neurocircuitos al enredar las neuronas y ceñir las conexiones entre ellas. Los investigadores querían saber si la diabetes relacionada con la obesidad está asociada con cambios estructurales en estos mosquiteros perineuronales y si éstos podrían tratarse.
El equipo de investigación notó que en el modelo de diabetes tipo 2 en ratas grasas Zucker Diabetes, estos mosquiteros son escasos en el hipotálamo en comparación con las ratas con niveles normales de azúcar en sangre. Sin embargo, en otras partes del cerebro los mosquiteros son normales.
Esta pérdida de redes perineuronales se revirtió rápidamente después de una única inyección de factor de crecimiento de fibroblastos 1 en el cerebro. La capacidad del factor de crecimiento de fibroblastos 1 para mejorar la diabetes se vio obstaculizada al eliminar las redes mediante digestión enzimática. Por el contrario, no se requieren redes perineuronales intactas para que el factor de crecimiento de fibroblastos 1 afecte la ingesta de alimentos.
Estos hallazgos identifican las redes perineuronales como objetivos clave para la remisión sostenida de la diabetes inducida por la acción del factor de crecimiento de fibroblastos 1. Los investigadores especulan que quizás estas redes ayuden a restringir la actividad de las neuronas Agrp y, por lo tanto, a bombear la señalización de la melanocortina.
Los investigadores planean continuar intentando cerrar la brecha entre las respuestas celulares (y extracelulares) al factor de crecimiento de fibroblastos 1 y la normalización de los niveles de azúcar en sangre. Esperan que esto pueda finalmente descubrir nuevas estrategias para lograr una remisión sostenida de la diabetes en los pacientes.