por SPIE
El cáncer de tiroides es el cáncer endocrino más común y afecta a más personas cada año a medida que aumentan las tasas de detección. Durante la escisión del tumor, los cirujanos suelen tener dificultades para determinar con exactitud la cantidad de tejido que se debe extirpar, ya que distinguir el cáncer del tejido sano en tiempo real es difícil y las estructuras cercanas son extremadamente delicadas.
Hoy en día, el diagnóstico y la evaluación de los márgenes se basan en la aspiración con aguja fina (PAAF) y la patología tradicional. Si bien son precisos, estos métodos son lentos, a veces inconcluyentes y no ofrecen una guía en tiempo real en el quirófano. Como resultado, los pacientes pueden someterse a cirugías innecesarias por nódulos benignos o requerir procedimientos adicionales si no se detecta tejido canceroso.
La Imagenología por Contraste Óptico Dinámico (DOCI) ofrece una forma radicalmente diferente de examinar el tejido. En lugar de utilizar colorantes o agentes de contraste, la DOCI ilumina el tejido y mide su autofluorescencia natural, la tenue luz emitida por las moléculas presentes en las células. El tejido sano y el canceroso brillan de forma diferente, creando firmas ópticas que pueden capturarse y analizarse. Cada escaneo DOCI recopila información de 23 canales ópticos diferentes en un amplio campo de visión, lo que produce un mapa detallado de la biología tisular con una rica huella espectral en muestras recién extirpadas.
En un estudio multiinstitucional publicado en Biophotonics Discovery , investigadores combinaron DOCI con aprendizaje automático para traducir estas complejas señales ópticas en información clínicamente significativa. En la Universidad de Duke, Tyler Vasse, en el laboratorio de Tuan Vo-Dinh, desarrolló un marco de análisis de IA en dos etapas. El despliegue y la aplicación clínica de la tecnología DOCI fueron llevados a cabo por Yazeed Alhiyari y miembros del equipo de Maie St. John en la Universidad de California, Los Ángeles.
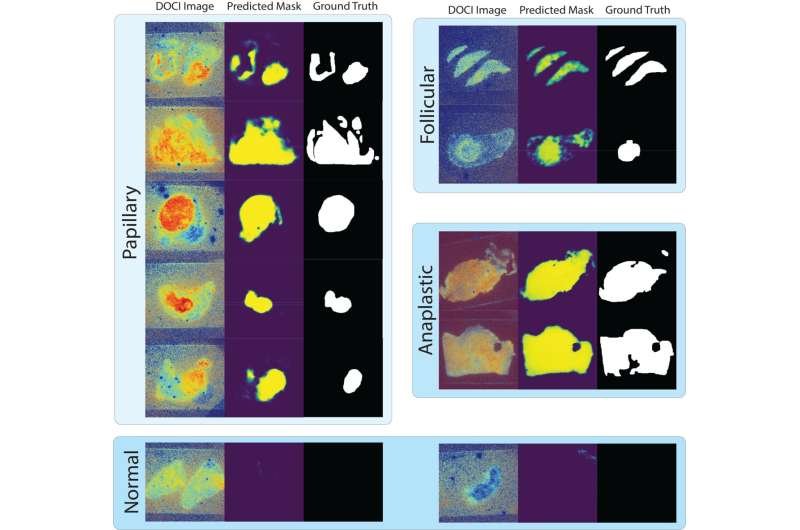
Biophotonics Discovery (2026). DOI: 10.1117/1.bios.3.1.015001
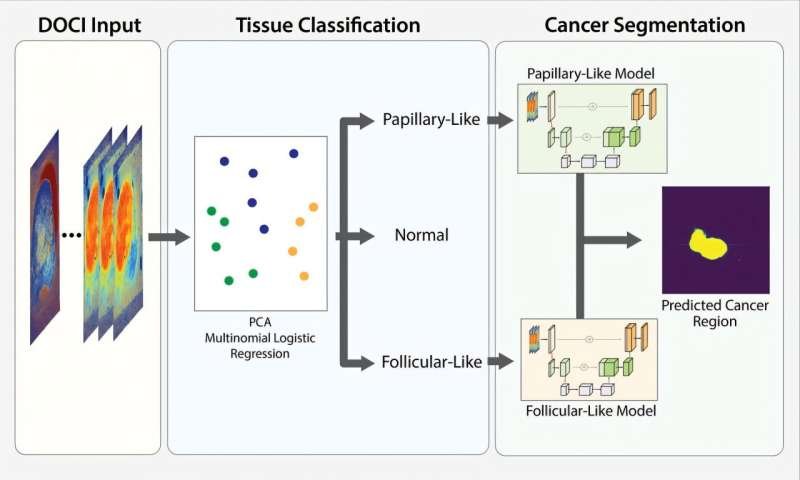
En la primera etapa, los investigadores emplearon un modelo de aprendizaje automático simple e interpretable para asignar cada muestra a una de tres categorías: tejido tiroideo sano, cáncer de tiroides folicular o cáncer de tiroides papilar, siendo estas dos últimas las neoplasias malignas tiroideas diferenciadas más comunes.
Al destilarse los 23 canales ópticos DOCI en un pequeño conjunto de características clave, el sistema clasificó con precisión las muestras en estas categorías, logrando una precisión perfecta en un conjunto de pruebas independiente. Cabe destacar que el modelo también identificó correctamente las muestras del subtipo anaplásico altamente agresivo como cancerosas, demostrando una amplia sensibilidad a los tejidos malignos.
La segunda etapa abordó una pregunta quirúrgica crucial: ¿dónde se encuentra exactamente el tumor? Para responderla, el equipo empleó modelos de aprendizaje profundo basados en la arquitectura U-Net, diseñada para identificar y mapear regiones específicas dentro de imágenes médicas. Con este enfoque, los modelos generaron mapas de probabilidad tumoral que resaltaron con precisión las regiones cancerosas, con un rendimiento especialmente bueno para el cáncer papilar de tiroides y tasas muy bajas de falsos positivos en tejido sin cáncer.
Aunque este trabajo analizó el tejido inmediatamente después de su extirpación, los resultados apuntan a un futuro en el que los cirujanos podrían recibir orientación rápida y sin etiquetas durante las operaciones. Al combinar la velocidad de la imagen óptica con el poder de la IA, DOCI tiene el potencial de reducir la incertidumbre en el quirófano, prevenir cirugías innecesarias, preservar el tejido sano y mejorar los resultados de los pacientes con cáncer de tiroides, permitiendo a los cirujanos ver el cáncer desde una nueva perspectiva.
Más información
Tyler Vasse et al., Segmentación y clasificación tumoral basada en aprendizaje automático mediante imágenes de contraste óptico dinámico para cáncer de tiroides, Biophotonics Discovery (2026). DOI: 10.1117/1.bios.3.1.015001
