Investigadores de la Facultad de Medicina de la Universidad Case Western Reserve y la Clínica Cleveland informan que el uso de acetato de medroxiprogesterona de depósito se asoció con un mayor riesgo relativo de diagnóstico de tumor cerebral meningioma en mujeres estadounidenses, con riesgo concentrado después de más de cuatro años de exposición o inicio a partir de los 31 años.
por Justin Jackson , Phys.org
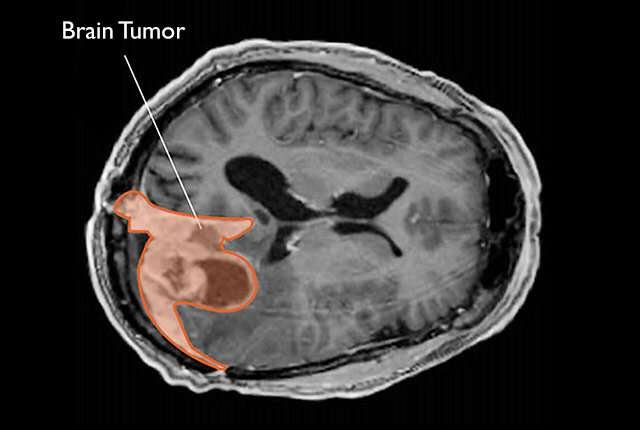
Los meningiomas son tumores cerebrales benignos que representan aproximadamente el 40 % de los tumores cerebrales primarios en EE. UU. y son más frecuentes en mujeres. El acetato de medroxiprogesterona de depósito es una progestina que se utiliza en mujeres como método anticonceptivo y para el tratamiento del sangrado uterino anormal o la endometriosis.
Probablemente debido al aumento de las tasas observadas en mujeres, estudios previos han examinado la exposición hormonal, con datos que indican la expresión del receptor de progesterona en muchos tumores y la del receptor de estrógeno en una proporción menor. Publicaciones de Francia y una base de datos de seguros de EE. UU. han vinculado la exposición al acetato de medroxiprogesterona de depósito con la cirugía o el diagnóstico de meningioma.
En el estudio, «Acetato de medroxiprogesterona de depósito y riesgo de meningioma en los EE. UU.», publicado en JAMA Neurology , los investigadores diseñaron un análisis de cohorte poblacional retrospectivo para examinar el riesgo relativo de diagnóstico de meningioma entre las usuarias de dMPA y otros anticonceptivos (incluidos oMPA, anticonceptivos orales combinados , DIU, píldoras de solo progestina e implantes subdérmicos).
Los datos provienen de TriNetX, una red estadounidense de 68 organizaciones de atención médica, que abarca desde diciembre de 2004 hasta diciembre de 2024. El total de mujeres elegibles fue de 61.588.239, con 10.425.438 pacientes que cumplieron con los requisitos de inclusión en los grupos de exposición y control.
Los tamaños de los grupos incluyeron control (n = 8.186.531), acetato de medroxiprogesterona de depósito (n = 88.668), acetato de medroxiprogesterona oral (n = 736.443), anticonceptivos orales combinados (n = 388.192), dispositivos intrauterinos (n = 614.666), DIU de cobre (n = 29.666), DIU de levonorgestrel de 52 mg (n = 180.035), DIU de levonorgestrel de 13,5/19,5 mg (n = 22.643), píldoras de progestina sola (n = 39.406) e implantes subdérmicos (n = 172.188).
Los análisis mostraron que las usuarias de acetato de medroxiprogesterona de depósito tenían un riesgo 143% mayor de diagnóstico de meningioma que los controles emparejados, con una incidencia de 7,39 por 100.000 pacientes-año en la cohorte de inyección y 3,05 en los controles.
La duración de la exposición indicó un riesgo 200% mayor entre cuatro y seis años de uso y un riesgo 290% mayor entre más de seis años.
Los estratos de edad de inicio indicaron un riesgo 277% mayor cuando se comienza entre los 31 y 40 años, 175% mayor entre los 41 y 50 años y 220% mayor cuando se comienza después de los 50 años.
El acetato de medroxiprogesterona oral mostró un riesgo 18% mayor en comparación con los controles.
No se observó un mayor riesgo con los anticonceptivos orales combinados, los DIU en general, las píldoras de progestina sola, los implantes subdérmicos, el DIU de cobre o el DIU de levonorgestrel de dosis baja.
Las estimaciones de riesgo reducido fueron un 26% menores para los anticonceptivos orales combinados, un 13% menores para los dispositivos intrauterinos en general y un 21% menores para el DIU de levonorgestrel de 52 mg.
Los investigadores concluyen que el uso de acetato de medroxiprogesterona de depósito se correlacionó con una mayor probabilidad de diagnóstico de meningioma , más evidente con más de cuatro años de exposición o cuando se inició después de los 31 años.
Más información: Tianqi Xiao et al., Acetato de medroxiprogesterona de depósito y riesgo de meningioma en EE. UU., JAMA Neurology (2025). DOI: 10.1001/jamaneurol.2025.3011
Gilles Reuter et al., Medroxiprogesterona de depósito y riesgo de meningioma, JAMA Neurology (2025). DOI: 10.1001/jamaneurol.2025.2973
