Si bien las vacunas pueden ser muy eficaces para prevenir virus, como el virus de la influenza A (IAV), suelen ser específicas de cada cepa y propensas a mutaciones de escape viral. El IAV por sí solo causa alrededor de 500.000 muertes en todo el mundo cada año. Para atender mejor a las poblaciones vulnerables y prevenir pandemias, los científicos han estado buscando maneras de crear terapias contra el IAV mejores, más universales, resistentes a las mutaciones y listas para usar.
por Krystal Kasal , Phys.org
Investigadores del Laboratorio Jackson en Farmington, Connecticut, podrían tener la solución. Su investigación, publicada recientemente en Science Advances , se centra en los anticuerpos no neutralizantes, que son proteínas producidas por el sistema inmunitario, mientras que otras terapias actuales con anticuerpos se centran en los anticuerpos neutralizantes. Las vacunas se basan en la creación de anticuerpos neutralizantes para prevenir la infección, pero los anticuerpos no neutralizantes funcionan ayudando al sistema inmunitario a combatir la infección; por lo tanto, la terapia con anticuerpos no neutralizantes no es una vacuna.
El equipo evaluó tres anticuerpos no neutralizantes que bloquean un canal de protones esencial (M2e) del virus de influenza aviar (VIA). Probaron diferentes variantes de los anticuerpos (en grupos de uno, dos o los tres) para determinar su eficacia profiláctica y terapéutica en modelos murinos con múltiples cepas del VIA, incluidas cepas de gripe aviar altamente letales. Descubrieron que la combinación de los tres anticuerpos, administrada en una especie de cóctel, resultó altamente eficaz.
Si bien las combinaciones de dosis bajas de pares M2e-mAb no lograron proteger completamente de la letalidad a los ratones expuestos al virus de la influenza A (IAV), una combinación triple de M2e-mAb con sitios de unión competitivos en la región N-terminal de la proteína M2 mostró una protección universal y una alta eficacia a dosis bajas. Estos resultados sugieren que la protección proporcionada por la combinación triple de M2e-mAb no se debe a un efecto dominante de uno o dos de los anticuerpos componentes, sino a la sinergia de los tres anticuerpos que componen la combinación M2e-mAb, escriben los autores del estudio.
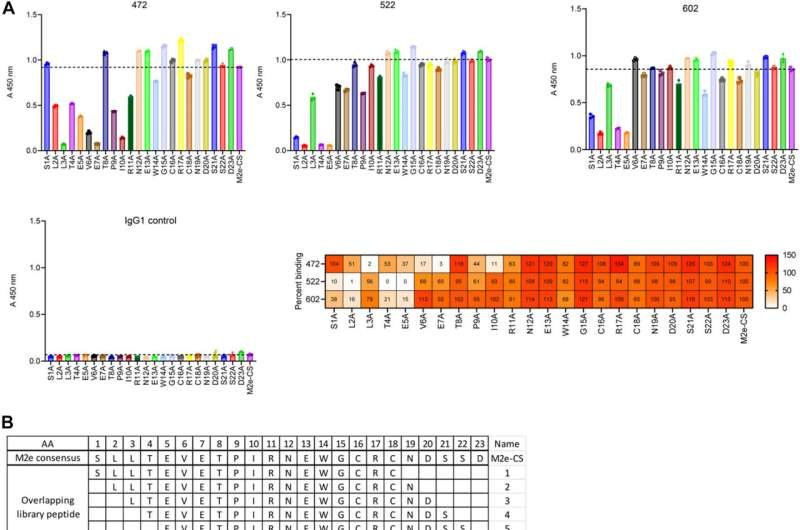
Science Advances (2025). DOI: 10.1126/sciadv.adx3505
La terapia fue eficaz incluso al administrarse en los primeros días de la infección. Descubrieron que el 100 % de los ratones infectados con la cepa de gripe aviar H7N9 sobrevivieron al ser tratados el día de la infección (día 0), el día siguiente (día 1) o el día 3 después de la infección. El 80 % de los ratones tratados el día 2 sobrevivieron.
A diferencia de los tratamientos con vacunas tradicionales, el tratamiento con cóctel de anticuerpos fue resistente a la mutación viral tanto en ratones inmunocompetentes como en inmunodeficientes.
Los autores del estudio escriben: «En conjunto, nuestros resultados han establecido la terapia triple de cóctel M2e-mAb como una terapia robustamente eficaz y resistente a mutantes de escape viral contra el virus de la influenza A (VIA), incluso contra uno de los subtipos de VIA más letales. Nuestros hallazgos contrastan marcadamente con los mAb M2e publicados previamente y los inhibidores de M2 aprobados por la FDA, que inducen rápidamente mutantes de escape en ratones WT e inmunodeprimidos».
Si bien la terapia es sumamente prometedora, aún necesita ser probada en humanos. Si resulta eficaz en ensayos con humanos , el tratamiento puede servir como una nueva terapia disponible y ampliamente efectiva para la gripe estacional y pandémica , especialmente cuando las nuevas versiones de las vacunas se retrasan o resultan ineficaces.
Más información: Teha Kim et al., Los anticuerpos no neutralizantes contra el ectodominio de la proteína de la matriz 2 de la influenza A son tratamientos ampliamente eficaces y resistentes a las mutaciones de escape viral, Science Advances (2025). DOI: 10.1126/sciadv.adx3505
